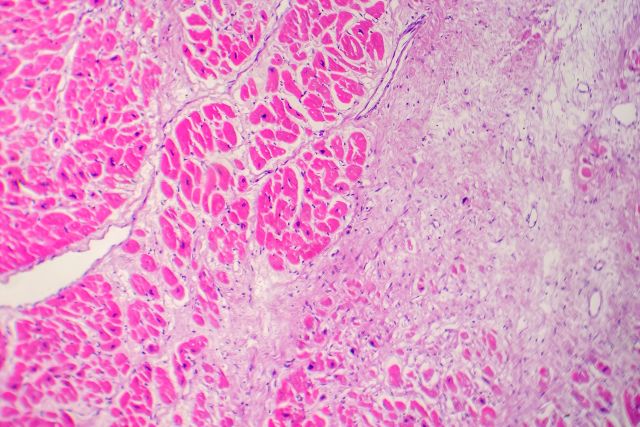
Ein neuer, bereits patentierter Therapieansatz scheint geeignet, die Bildung von überschüssigem Narbengewebe nach Herzinfarkt zu verhindern: die Blockade des TF-PAR2-Signalwegs, der bei herzschädlichen Entzündungsreaktion eine wichtige Rolle spielt.
Nach einem Infarkt muss nekrotisches Myokardgewebe abgebaut werden, was mit Entzündungsreaktionen einhergeht. Doch was „gut gemeint“ ist, kann zum Bumerang werden: Überschießende Entzündungen können zur Fibrosierung und Vernarbung führen und so die Elastizität und Pumpkraft des Herzens dauerhaft beeinträchtigen. Dabei können Entzündungen auch gesundes Gewebe erfassen und schädigen.
Profibrotischer Signalweg
Philip Wenzel und sein Team von der Universitätsmedizin Mainz haben herausgefunden, dass der TF-PAR2-Signalweg eine Schlüsselrolle bei diesen kontraproduktiven Prozessen spielt. Der Gewebefaktor (Tissue Factor, TF) und sein Rezeptor (Protease-aktivierter Rezeptor 2, PAR2) tragen maßgeblich zu einer Überaktivierung von Monozyten bei, die aus dem Blut ins Herz einwandern und dort als Fresszellen geschädigtes Gewebe entsorgen. Diese Aufräumarbeiten gehen mit heftigen Entzündungen einher. Auf den Plan gerufene Fibroblasten vollenden den bindegewebigen Umbau des Herzens.
Durch die Blockade des identifizierten Signalwegs sollte sich das Remodeling des Herzens reduzieren lassen, so die logische Schlussfolgerung. Sowohl gerinnungshemmende Medikamenten als auch spezifische monoklonale Antikörper wären geeignete Ansätze. Und es funktioniert tatsächlich: Am Mausmodell dämmte die Blockade der Signalübertragung überschießende Gerinnungs- und Entzündungsreaktionen ein, es wurde weniger Wachstumsfaktor TGF-ß1 produzierte, und die Fibrosierung des Herzgewebes wurde begrenzt. Vernarbungen ließen sich so um 50 % reduzieren, und die Pumpleistung ließ sich stabilisieren, was mit einer geringeren Sterblichkeit einherging. Alle behandelten Tiere überlebten, während in der Kontrollgruppe 40 Prozent der Tiere starben.
Europäisches Patent erteilt
Auf den innovativen Ansatz wurde nun das Europäische Patent EP4247408 erteilt. Im nächsten Schritt gilt es nun, Investoren zu gewinnen, die in die Weiterentwicklung einsteigen. Eingeschlossen in das Patent sind neu entdeckte Biomarker, darunter das profibrotisch wirksame TGF-ß1 im Blut. „Mit diesen Biomarkern können wir frühzeitig sehen, welche Patienten ein höheres Risiko für eine schwere Herzschwäche haben – und sie gezielt behandeln“, so Wenzel.
Besonders Herzinfarktpatienten, bei denen keine Reperfusionstherapie erfolgt, dürften von dem innovativen Ansatz profitieren. Bei Frauen ist dies unverhältnismäßig häufig der Fall, weil sich der weibliche Herzinfarkt oft mit unspezifischen Symptome wie Übelkeit, Schweißausbrüche, Atemnot und Rückenschmerzen manifestiert und deshalb oft – für eine Reperfusionstherapie – zu spät erkannt wird. „Es ist absurd, sagt Wenzel, „dass diese Beschwerden als atypisch gelten. Frauen sind keine Ausnahme!“
Quelle: Pressemitteilung des Deutschen Zentrums für Herz-Kreislauf-Forschung (DZHK) vom 17. Februar 2025